特别声明:本产品及我公司所售其他产品均为科研类试剂产品,严禁用于药物、YL及其他非科研用途。
北京百奥莱博生产销*(代"售")的副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒(TLH)批发,是高品质的细菌PCR检测试剂盒产品,欢迎的您垂询订购。
名称:副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒(TLH)批发
等级:科研试剂
编号:SYA070
规格:48次/盒
品Pai:百奥莱博
产地:国产|进口
一、简介:
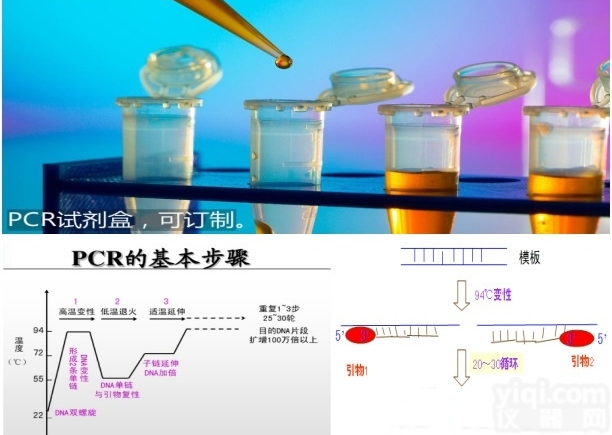
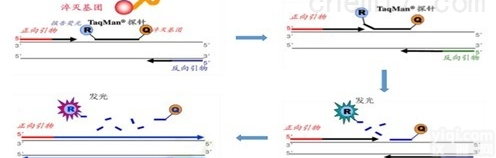
本试剂盒用一对副溶血性弧菌不耐热溶血毒素特异性引物,结合一条特异性探针,用荧光PCR技术对副溶血性弧菌不耐热溶血毒素的核酸进行体外扩增检测,用于临床上对可疑感染者的病原学诊断。
二、用途:
该试剂盒适用于检测水样粪便、疑似污染的水、食物等样本中的副溶血性弧菌不耐热溶血毒素(TLH),用于副溶血性弧菌不耐热溶血毒素(TLH)感染的辅助诊断,其检测结果仅供临床参考。
三、试剂盒组成:(48T)
| 组份 | 数量 | 规格 |
| TLH反应液(TLH-qPCR MIX) | 1管 | 672μL/管 |
| DNA抽提液(DNA Extraction) | 2管 | 1.5mL/管 |
| 酶混合物(Enzymes MIX) | 1管 | 48μL/管 |
| 阴性对照(NTC) | 1管 | 50μL/管 |
| TLH阳性对照(TLH -PTC) | 1管 | 50μL/管 |
四、
荧光PCR 仪器适用范围ABI系列、MJ系列、Roche系列,博日系列及其他荧光定量PCR 检测仪。
五、
储存条件及有效期:本试剂盒于-20℃以下保存,有效期为6个月。
六、
样品采集、前处理与DNA 提取6.1 样品采集
水样便取0.5-1 mL;疑似污染的食物取1g。
6.2 样本前处理:
水样便13000rpm离心2min,去尽上清;疑似污染的食物用手术剪剪碎混匀后取0.05g于研磨器中研磨,加入1.5mL生理盐水后继续研磨,待匀浆后转至1.5mL灭菌离心管中,8000rpm离心2min,取上清液100μL于1.5mL灭菌离心管中;疑似污染的水直接取100μL。
6.3
DNA提取可采用PCR试剂盒配备的DNA抽提液,按以下说明进行DNA核酸的粗提。也可采购北京百奥莱博科技有限公司生产的(DNA提取试剂盒(过柱法-荧光配套),并按照相应试剂盒说明进行操作。
对上述处理好的样本加入50uL核酸提取液,100℃恒温处理10min,13000rpm离心5min,取上清液转移至新的1.5mL EP管,-20℃保存;
注:阳性对照和阴性对照为已经抽提好的核酸(无需提取),直接取5μL加入到反应体系中即可。
由于阳性对照浓度较高,建议ZH在样品制备区域加入阳性对照。
七、
检测步骤:7.1
试剂的准备从试剂盒中取出荧光PCR 反应液(TLH-qPCR MIX)、酶混合液(Enzymes MIX),冰上融化并振荡混匀后,10000rpm 离心10s。
设所需要的PCR 反应管管数为N(N=样本数+1 管阴性对照+1 管阳性对照),每个测试反应体系配制如下表:
| 试剂 | 每个反应加入的量 | N个反应加入的量 |
| 荧光PCR反应液 | 14µL | N×14µL |
| 酶混合液 | 1µL | N×1µL |
| 总量 | 15µL | N×15µL |
计算好各试剂的使用量,加入一适当体积洁净离心管中,充分混匀,10000rpm 离心10s,向设定的N 个PCR 反应管中分别加入15μL 荧光PCR 反应液,向每管中加入处理后样品/阴性对照(NTC)/阳性对照(TLH-PTC)5μL,10000rpm 瞬时离心10 秒。
7.2
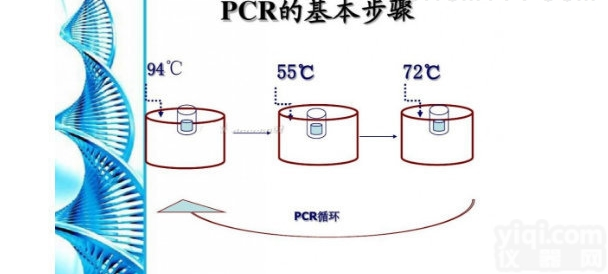
qPCR反应条件将各反应管放入实时荧光PCR仪器的反应槽内。推荐循环条件:
| | 1循环 | 50℃ for 2 min |
| 预变性 | 1循环 | 95℃ for 10 min |
| PCR扩增 | 40循环 | 95℃ for 15 sec
60℃ for 60 sec |
在60℃延伸时收集荧光信号。报告基团:设置为FAM。淬灭基团:NONE,请勿选择ROX参比荧光。
八、
结果分析:8.1
结果分析条件设定直接读取检测结果。基线和阈值设定原则根据仪器噪声情况进行调整,以阈值线刚好超过正常阴性样品扩增曲线的ZG点为准。
8.2
试验成立判定(1)阴性对照(NTC):不应产生任何的扩增曲线。
(2)阳性对照(TLH-PTC):均产生扩增曲线。
(3)以上条件应同时满足,否则,此次试验视为无效。
8.3
结果判定(1)在试验成立的条件下,Ct值≤35的样本为阳性,表明副溶血性弧菌不耐热溶血毒素核酸阳性。
(2)Ct值显示为无的样本为阴性样本,表明副溶血性弧菌不耐热溶血毒素核酸阴性。
(3)如果Ct值>35,判为可疑样品。对于可疑样品,先看扩增曲线。如果扩增曲线为对数扩增曲线,则为可疑阳性,否则判为阴性。
(4)对于可疑阳性样品,重新抽提核酸,再次进行副溶血性弧菌不耐热溶血毒素qPCR检测。如果重复扩增曲线为对数扩增曲线,判为样本阳性,表明副溶血性弧菌不耐热溶血毒素核酸阳性;否则判为样本阴性。
九、
注意事项:(1)初次使用前请仔细阅读说明书。并严格按照说明书步骤操作。
(2)所有使用的离心管应高压灭菌,而且必须不含DNA 酶。
(3)PCR 操作应严格按照要求分区(试剂配制区、标本处理区、PCR 扩增区等),防止实验室污染。
(4)样本提取、试剂配置、加样需在不同区的超净工作台进行,以免污染。
(5)试剂盒里所有物品应视为污染物对待,并按照卫生部《微生物生物医学实验室生物安全通则》进行处理。
.jpg)
我公司的
副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒(TLH)批发,性价比高,货期短,送货上门,欢迎您来电咨询购买,另外,我公司还生产供应销*(代"售")下列产品:
·冠状病毒(NL63)单重荧光PCR检测试剂盒
编号:SYA182
等级:科研实验专用
规格:48次/盒
·卵形疟原虫单重荧光PCR检测试剂盒
编号:SYA126
等级:科研实验专用
规格:48次/盒
一、
简介:本试剂盒用一对卵形疟原虫特异性引物,结合一条特异性荧光探针,用荧光PCR探针技术进行卵形疟原虫的检测。
二、
用途:本试剂盒可用于卵形疟原虫检测鉴定及突发公共卫生事件的处置,还可用于卵形疟原虫的环境监测、卫生检疫及感染的辅助诊断,其检测结果仅供临床参考。
三、
试剂盒组成:(48T)
组份 数量 规格
卵形疟原虫荧光PCR反应液(qPCR MIX) 1管 672μL/管
DNA抽提液(DNA Extraction) 2管 1.5mL/管
酶混合物(DNA Polymerase MIX) 1管 48μL/管
阴性对照(NTC) 1管 50μL/管
卵形疟原虫阳性对照(PTC) 1管 50μL/管
四、
荧光PCR 仪器适用范围ABI 系列,Bio-Rad 系列,Roche 系列等荧光定量PCR 检测仪等。
五、
储存条件及有效期:本试剂盒于-20℃保存,避免反复冻融,有效期为6 个月。
六、实验操作步骤
6.1 标本采集
血液: 用一次性无菌5ml 注射器抽取疑似人或动物血3-5ml,置于枸橼酸*或EDTA2Na 抗凝管中,摇匀送检。
肺脏等组织:取上述组织1g左右,置于1.5ml洁净EP管中送检。
乳液、体液等标本:取相应标本3-5ml,转至1.5ml洁净EP管中送检。
6.2
DNA提取可采用PCR试剂盒配备的DNA抽提液,按以下说明进行DNA核酸的粗提。也可采购北京百奥莱博科技有限公司生产的DNA提取试剂盒(过柱法-荧光配套)或其他合适的商业化产品,并按照相应试剂盒说明进行操作。
血液样本:直接取200μl 抗凝血,转至一洁净的1.5ml 离心管中,加入1ml 双蒸水,剧烈震荡30s,8000rpm 离心5min,弃上清,至无明显红色沉淀。(若沉淀明显,请再重复上述步骤一次)。加入1ml生理盐水,剧烈震荡15s,13000rpm 离心5min,弃上清。沉淀加入50μl 核酸提取液(使用前请室温溶解并充分混匀)并与沉淀混匀,100℃恒温10min,13000rpm 离心3min,取上清4μl 进行PCR 反应。
肺、淋巴结等固体组织:剪取约0.1g 组织,用生理盐水洗去血污,剪碎加入0.5mL TE 转移到匀浆器中匀浆。将匀浆液50μl 转移到1.5mL 离心管中,加入50μl 核酸提取液(使用前请室温溶解并充分混匀)并与沉淀混匀,100℃恒温10min,13000rpm 离心3min,取上清4μl 进行PCR 反应。
乳液等液体标本:取标本2-3mL,13000rpm 离心3min,弃上清,沉淀加入50μl 核酸提取液(使用前请室温溶解并充分混匀)并与沉淀混匀,100℃恒温10min,13000rpm 离心3min,取上清4μl进行PCR 反应。
注:阳性对照和阴性对照为已经抽提好的核酸(无需提取),直接取5μL 加入到反应体系中即可。由于阳性对照浓度较高,建议ZH在样品制备区域加入阳性对照。
七、
检测步骤:7.1 PCR 扩增
从试剂盒中取出荧光PCR 反应液(卵形疟原虫-qPCR MIX)、酶混合物(DNA Polymerase MIX),室温融化并振荡混匀后,10000rpm 离心10s。
设所需要的PCR 反应管管数为N(N=样本数+1 管阴性对照+1 管阳性对照),每个测试反应体系配制如下表:
试剂 每个反应加入的量 N个反应加入的量
荧光PCR反应液 14µL N×14µL
酶混合液 1µL N×1µL
总量 15µL N×15µL
计算好各试剂的使用量,加入一适当体积洁净离心管中,充分混匀,10000rpm 离心10s,向设定的N 个PCR 反应管中分别加入15μL,向每管中加入处理后样品或阴性对照(NTC)和阳性对照(PTC)5μL,10000rpm 瞬时离心10秒。
7.2
qPCR反应条件将各反应管放入定量PCR仪器的反应槽内。
推荐循环条件:
1循环 50℃ for 2 min
预变性 1循环 95℃ for 10 min
PCR扩增 40循环 95℃ for 15 sec
60℃ for 60 sec
在60℃延伸时收集荧光信号。报告基团:设置为FAM。淬灭基团:NONE,请勿选择ROX参比荧光。
八、
结果分析:8.1
结果分析条件设定直接读取检测结果。基线和阈值设定原则根据仪器噪声情况进行调整,以阈值线刚好超过正常阴性样品扩增曲线的ZG点为准。
8.2
试验成立判定阴性对照(NTC):不应产生任何的扩增曲线。
阳性对照(PTC):均产生扩增曲线。
以上条件应同时满足,否则,此次试验视为无效。
8.3
结果判定在试验成立的条件下,Ct值≤35的样本为阳性,表明卵形疟原虫核酸阳性。
Ct值显示为无的样本为阴性样本,表明卵形疟原虫核酸阴性。
如果35<Ct值≤40,判为可疑样品。对于可疑样品,先看扩增曲线。如果扩增曲线为对数扩增曲线,则为可疑阳性,否则判为阴性。
对于可疑阳性样品,重新抽提核酸,再次进行卵形疟原虫real time PCR检测。如果重复扩增曲线为对数扩增曲线,判为样本阳性,表明卵形疟原虫核酸阳性;否则判为样本阴性。
九、
注意事项:(1)初次使用前请仔细阅读说明书。并严格按照说明书步骤操作。
(2)所有使用的离心管应高压灭菌,而且必须不含DNA酶。
(3)PCR操作应严格按照要求分区(试剂配制区、标本处理区、PCR 扩增区等),防止实验室污染。
(4)样本提取、试剂配置、加样需在不同区的超净工作台进行,以免污染。
(5)试剂盒里所有物品应视为污染物对待,并按照卫生部《微生物生物医学实验室生物安全通则》进行处理。
副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒(TLH)批发关键词:百奥莱博,TLH,副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒,副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒(TLH),SYA070
.jpg)
9032-75-1 PectolyaseY-23 果胶酶Y-23
总胆红素(TBIL)检测试剂盒(BOD比色法) 50T
1kb DNA Ladder Ⅱ Urease(jack bean)
C1401 小牛血清(无菌过滤)
BTN80803 柱式动物线粒体DNAOUT,PCR级 Column Animal mtDNAOUT,PCR Grade
吡*(代"啶")盐*(代"酸")盐 MBHA resin 628-13-7
134-58-7 8-氮杂鸟嘌呤 8-Azaguanine(原装)
还原辅酶ⅠYZ剂 Trypan blue
N-乙酰-神经*酸 Amberlite XAD2 131-48-6
ARB14118 猪CD4分子(CD4)血清中含量检测
硝酸盐还原实验试剂 2×50ml
ARB11823 人精*酸酶(Arg)elisa测定使用说明书 Human arginase,arg ELISA KIT
68-19-9 维生素B12 VitaminB12
GXRNA保存液 100ml
角鲨烯 4-Hydroxybenzoic acid sodiu*(代"m") salt 111-02-4
C0201 特级新生牛血清(无菌过滤) 100ml/200ml/500ml/500ml*20瓶
F030310 胶体金标记羊抗乙肝表面抗原抗体 Polyclonal Goat Anti-HBsAg*GOLD
BTN90510 包涵体大量纯化试剂盒 Inclusion Body Maxiprep Kit
BL0864 羊抗人C3免疫血清
副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒(TLH)批发关键词:百奥莱博,TLH,副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒,副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒(TLH),SYA070
.jpg)
·猪伪狂犬病毒抗体ELISA检测试剂盒
编号:SYA630
等级:科研实验专用
规格:192次/盒
·猪流行性腹泻病毒单重荧光PCR检测试剂盒
编号:SYA779
等级:科研实验专用
规格:48次/盒
一、
简介:本试剂盒用一对猪流行性腹泻病毒特异性引物,结合一条特异性荧光探针,用一步法荧光RT-PCR技术对猪流行性腹泻病毒RNA进行体外扩增检测,用于临床上对可疑感染者的病原学诊断。本试剂盒中猪流行性腹泻病毒的探针报告基团为FAM。
二、
用途:本试剂盒适用于病猪血液、肠系膜淋巴结、扁桃体、肠组织(空肠中段)、肠内容物以及粪便等标本中的猪流行性腹泻病毒(PEDV)特异性检测。适用于猪流行性腹泻病毒(PEDV)感染的辅助诊断、监测及流行病学调查,其检测结果仅供临床参考。
三、
试剂盒组成:(48T)
组份 数量 规格
猪流行性腹泻病毒反应液(PEDV-qRT-PCR MIX) 1管 672μL/管
酶混合物(Enzymes MIX) 1管 48μL/管
无核酸酶水(Nuclease-Free Water) 1管 500μL/管
阴性对照(NTC) 1管 50μL/管
阳性对照(PEDV-PTC) 1管 50μL/管
四、
储存条件及有效期:本试剂盒于-20℃以下保存,有效期为6个月。
五、
荧光PCR仪器适用范围:ABI系列,Roche系列等荧光定量PCR检测仪等。
六、
样品的采集与RNA提取6.1
样品的采集按照相关标准采集。标本短期内可保存于-20℃,长期保存可置-80℃,但不能超过6个月,标本运送应采用0℃冰壶。
6.1.1 血清:用一次性无菌注射器抽取静脉血2mL,注入无菌的干燥玻璃管,室温(22-25℃)放置30-60min,血标本可自发完成凝集析出血清,或直接使用水平离心机,3000rpm离心5min,吸取上层血清,转移至1.5mL灭菌离心管中备用。
6.1.2 血浆:用一次性无菌注射器抽取静脉血2mL,注入含EDTA2Na(乙二*(代"胺")四乙酸二*)或柠檬酸*抗凝剂的玻璃管,立即轻轻颠倒玻璃管混合5-10次,使抗凝剂与静脉血充分混匀,5-10min后即可分离出血浆,转移至1.5mL灭菌离心管中备用。
6.1.3 拭子、分泌物等样品:在装有拭子或分泌物的离心管中加入500µL PBS或生理盐水,剧烈振荡30s。棉拭子尽量挤出液体转移到无DNA酶污染的离心管中备用。
6.1.4 病灶组织样品:称取组织约0.1g于研磨器或组织匀浆器中研磨(置于冰上或加入液氮),再加1mL生理盐水研磨至无块状物,然后将样品转至1.5mL灭菌离心管中备用。
6.2
RNA提取可采购北京百奥莱博科技有限公司生产的RNA提取试剂盒(过柱法-荧光配套)或其他合适的商业化产品,并按照相应试剂盒说明进行操作。
注:阳性对照和阴性对照为已经抽提好的核酸(无需提取),直接取5µL加入到反应体系中即可。由于阳性对照浓度较高,建议ZH在样品制备区域加入阳性对照。
七、
检测步骤:7.1
试剂的准备从试剂盒中取出荧光qRT-PCR反应液(PEDV-qRT-PCR MIX)、酶混合物(Enzymes MIX),冰上融化并振荡混匀后,10000rpm离心10s。
设所需要的PCR反应管管数为N(N=样本数+1管阴性对照+1管阳性对照),每个测试反应体系配制如下表:
试剂 每个反应加入的量 N个反应加入的量
荧光PCR反应液 14µL N×14µL
酶混合物 1µL N×1µL
总量 15µL N×15µL
计算好各试剂的使用量,加入一适当体积洁净离心管中,充分混匀,10000rpm离心10s,向设定的N个PCR反应管中分别加15μL,向每管中加入处理后样品/阴性对照(NTC)/阳性对照(PEDV-PTC)5μL,10000rpm瞬时离心10秒。
7.2
qRT-PCR反应条件将各反应管放入实时荧光PCR仪器的反应槽内。
推荐循环条件:
反转录(Reverse Transcription) 1循环 45℃ for 10 min
预变性 1循环 95℃ for 10 min
PCR扩增 40循环 95℃ for 15 sec
60℃ for 45 sec
在60℃延伸时收集荧光信号。报告基团:设置为FAM,淬灭基团:NONE,请勿选择ROX 参比荧光。
八、结果分析
8.1
结果分析条件设定直接读取检测结果。基线和阈值设定原则根据仪器噪声情况进行调整,以阈值线刚好超过正常阴性样品扩增曲线的ZG点为准。
8.2
试验成立判定(1) 阴性对照(NTC):不应产生任何的扩增曲线。
(2) 阳性对照(PEDV-PTC):均产生扩增曲线。
(3) 以上条件应同时满足,否则,此次试验视为无效。
8.3
结果判定(1) 在试验成立的条件下,Ct值≤35的样本为阳性,表明PEDV核酸阳性。
(2) Ct值显示为无的样本为阴性样本,表明PEDV核酸阴性。
(3) 如果35<Ct值≤40,判为可疑样品。对于可疑样品,先看扩增曲线。如果扩增曲线为对数扩增曲线,则为可疑阳性,否则判为阴性。
(4) 对于可疑阳性样品,重新抽提核酸,再次进行PEDV qRT-PCR检测。如果重复扩增曲线为对数扩增曲线,判为样本阳性,表明PEDV核酸阳性;否则判为样本阴性。
九、
注意事项:(1) 初次使用前请仔细阅读说明书。并严格按照说明书步骤操作。
(2) 所有使用的离心管高压灭菌,而且必须不含RNA酶。
(3) PCR操作应严格按照要求分区(试剂配制区、标本处理区、PCR扩增区等),防止实验室污染。
(4) 样本提取、试剂配置、加样需在不同区的超净工作台进行,以免污染。
(5) 试剂盒里所有物品应视为污染物对待,并按照卫生部《微生物生物医学实验室生物安全通则》进行处理。
.jpg)
我公司正在优惠促销细菌PCR检测试剂盒等系列产品,期待您的咨询选购副溶血性弧菌不耐热溶血毒素荧光PCR检测试剂盒(TLH)批发。
温馨提示:不可用于临床ZL。

.jpg)
.jpg)
.jpg)
.jpg)