 Hieff Mut™Site-Directed Mutagenesis Kit 定点突变试剂盒
Hieff Mut™Site-Directed Mutagenesis Kit 定点突变试剂盒
 Hieff Mut™Site-Directed Mutagenesis Kit 定点突变试剂盒
Hieff Mut™Site-Directed Mutagenesis Kit 定点突变试剂盒
 Hieff Mut™ Site-Directed Mutagenesis Kit定点突变试剂盒
Hieff Mut™ Site-Directed Mutagenesis Kit定点突变试剂盒
 Hieff Mut™Site-Directed Mutagenesis Kit 定点突变试剂盒
Hieff Mut™Site-Directed Mutagenesis Kit 定点突变试剂盒
 现货...Agilent/安捷伦 210518 QuikChange Lightning Site-Directed Mutagenesis Kit 定点突变试剂盒 单点突变试剂盒(适用于各种大小的质粒<14kb) 10 rxn
现货...Agilent/安捷伦 210518 QuikChange Lightning Site-Directed Mutagenesis Kit 定点突变试剂盒 单点突变试剂盒(适用于各种大小的质粒<14kb) 10 rxn
 人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA 试剂盒 人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA 试剂盒供应商
人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA 试剂盒 人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA 试剂盒供应商
 人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA试剂盒人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA Kit的价格
人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA试剂盒人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA Kit的价格
 人抗突变型瓜氨酸波形蛋白抗体 (MCV)ELISA试剂盒人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA Kit的价格
人抗突变型瓜氨酸波形蛋白抗体 (MCV)ELISA试剂盒人抗突变型瓜氨酸波形蛋白抗体(MCV)ELISA Kit的价格
 人ELISA试剂盒,人抗突变型瓜氨酸波形蛋白抗体ELISA试剂盒说明书
人ELISA试剂盒,人抗突变型瓜氨酸波形蛋白抗体ELISA试剂盒说明书
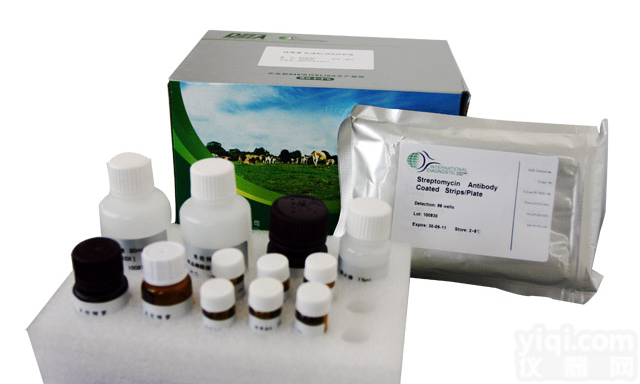 MCVELISA试剂盒 人抗突变型瓜氨酸波形蛋白抗体 ELISA试剂盒
MCVELISA试剂盒 人抗突变型瓜氨酸波形蛋白抗体 ELISA试剂盒
 MCV试剂盒,人抗突变型瓜氨酸波形蛋白抗体Elisa试剂盒
MCV试剂盒,人抗突变型瓜氨酸波形蛋白抗体Elisa试剂盒
 Elisa试剂盒之人突变型瓜氨酸波形蛋白抗体(MCV)Elisa试剂盒
Elisa试剂盒之人突变型瓜氨酸波形蛋白抗体(MCV)Elisa试剂盒
本产品信息由(上海翊圣生物科技有限公司)为您提供,内容包括(Hieff Mut™Site-Directed Mutagenesis Kit 定点突变试剂盒)的品牌、型号、技术参数、详细介绍等;如果您想了解更多关于(Hieff Mut™Site-Directed Mutagenesis Kit 定点突变试剂盒)的信息,请直接联系供应商,给供应商留言。若当前页面内容侵犯到您的权益,请及时告知我们,我们将马上修改或删除。